Synthetische Gestagene
Gestagene zählen zu den Sexualhormonen. Aufgrund ihrer ovulationshemmenden Wirkung bei Frauen sind synthetische Gestagene der Hauptbestandteil hormoneller Kontrazeptiva. Auch in der Hormonersatztherapie kommen sie häufig zum Einsatz und dienen der Endometriumprotektion. Darüber hinaus werden bestimmte Gestagene zur Behandlung der Endometriose eingesetzt.1,2,3
Was sind Gestagene?
Der Begriff „Gestagen“ umfasst eine ganze Reihe von Sexualsteroiden, darunter natürliche Gestagene wie Progesteron und Dydrogesteron (ein Stereoisomer von Progesteron) sowie diverse synthetische Verbindungen. Im Gegensatz zu den natürlichen Varianten weisen synthetische Gestagen eine längere Halbwertszeit auf. Sie besitzen außerdem unterschiedliche Partialwirkungen und sind in verschiedenen Darreichungsformen verfügbar.1,2
Anwendungsgebiete von Gestagenen
Gestagene werden in der klinischen Praxis insbesondere zur Behandlung von Frauen im fertilen Alter sowie in der Peri- und Postmenopause eingesetzt. In Form von Gestagenmonotherapien dienen sie beispielsweise der Zyklusregulierung sowie der hormonellen Kontrazeption. Verfügbare Applikationsformen zur Kontrazeption sind estrogenfreie Pillen (auch: Gestagenpillen, „progestogen only pill“, POP), Hormonspiralen sowie die sogenannte „Dreimonatsspritze“.1,2,3
Außerdem werden Gestagene häufig in Kombination mit einem Estrogen verwendet. Entsprechende Präparate sind klassische kombinierte hormonelle Kontrazeptiva (KHK) sowie kombinierte Präparate zur Hormonersatztherapie (HRT) für peri- und postmenopausale Frauen.1,2,3
Darüber hinaus werden Gestagene entweder als Monotherapie oder in Form eines KHK auch zur Therapie der Endometriose eingesetzt.4,5 In Deutschland ist bislang nur das Gestagen Dienogest als orales Präparat hierfür zugelassen.6 Andere hormonelle Therapien mit einem Gestagenmonopräparat oder einem KHK stellen einen Off-label-Use dar. Wird ein kombiniertes Präparat gewählt, so haben sich insbesondere einphasige kombinierte orale Kontrazeptiva (KOK) im Langzyklus zur Linderung der Endometriose-bedingten Schmerzen als gut wirksam und nebenwirkungsarm erwiesen. Eingesetzt werden aber auch andere Applikationsformen wie zum Beispiel Hormonspiralen (Levonorgestrel-Intrauterindevice, LNG-IUD) oder Vaginalringe.5
Einteilung der Gestagene
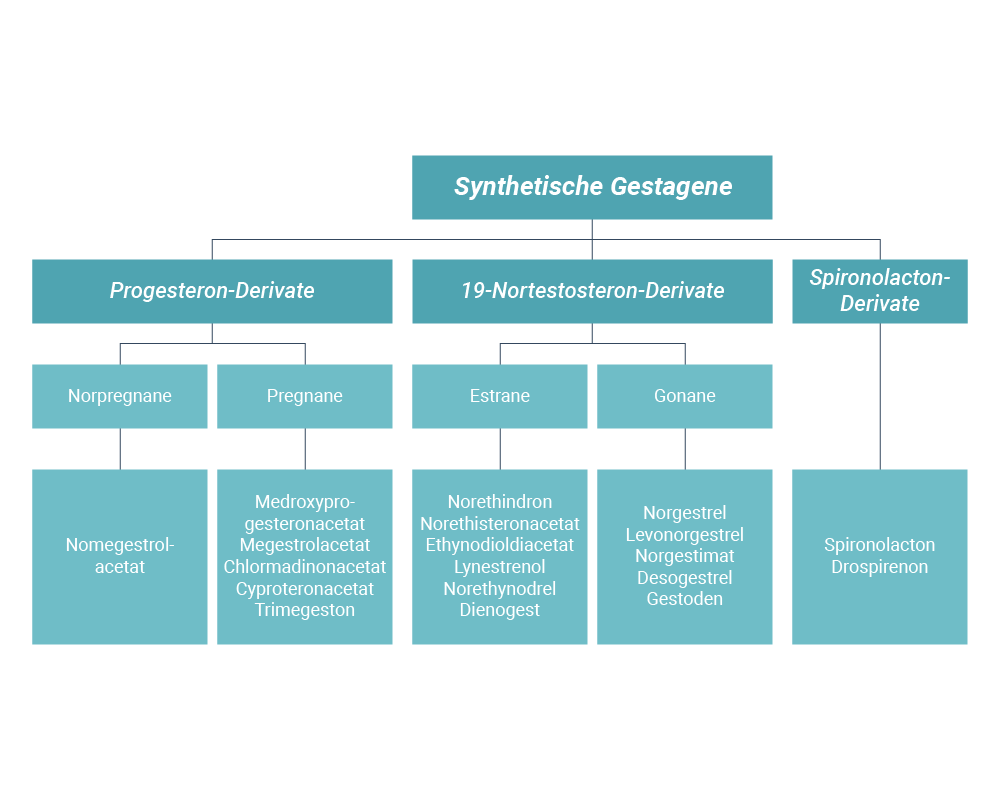
Die Struktur der synthetischen Gestagene ähnelt der des natürlichen Progesterons. Daher wirken synthetische Gestagene und Progesteron ähnlich, weisen jedoch auch Unterschiede in ihrer Wirksamkeit auf. Chemisch leiten sich die synthetischen Gestagene überwiegend von Progesteron bzw. 17α-Hydroxyprogesteron (17α-OH-Progesteron, 17-OHP) oder Testosteron ab. Erstere werden als 19-Norprogesteron-Derivate bzw. 17α-OH-Progesteron-Derivate bezeichnet und die von Testosteron abgeleiteten Gestagene als 19-Nortestosteron-Derivate. Letztere verlieren durch das Einführen einer Ethinylgruppe an Position C17α ihre androgene Wirkung zugunsten einer gestagenen Aktivität.1,3,4
Zur Gruppe der Progesteron-Derivate zählen die von 19-Norprogesteron abgeleiteten Norpregnane sowie die von 17α-OH-Progesteron abgeleiteten Pregnane. Die 19-Nortestosteron-Derivate werden wiederum in die sogenannten Estrane und die Gonane eingeteilt. Ein weiteres synthetisches Gestagen ist das Spironolacton-Derivat Drospirenon (s. Abb. 1).1,2,4
Wie wirken Gestagene?
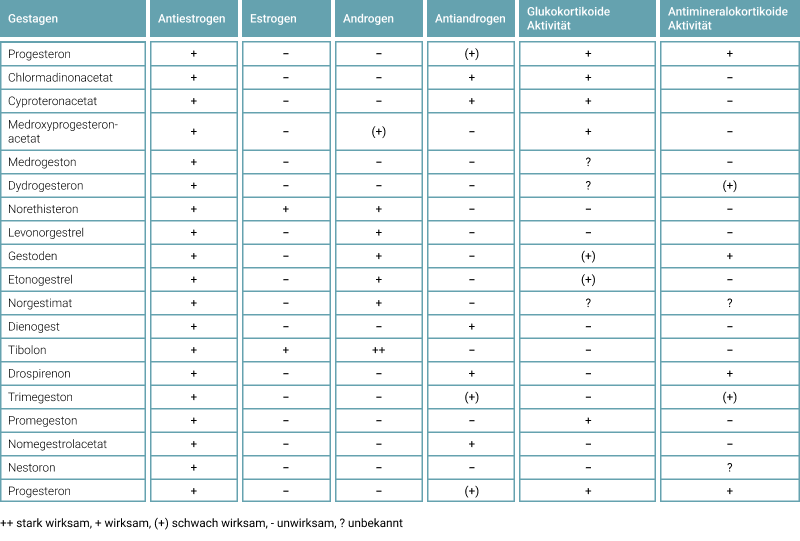
Ihre Wirkung vermitteln Gestagene einerseits durch Bindung an den beiden nuklearen Progesteronrezeptoren (PRA und PRB) sowie zusätzlich durch Interaktion mit membranären Bindungsstellen. Letztere sind dadurch gekennzeichnet, dass die endokrine Signalvermittlung viel schneller erfolgt. Synthetische Gestagene docken, je nach Molekül, aber auch an anderen Steroidrezeptoren an und besitzen dadurch ein breites Spektrum an Partialwirkungen, die sie vom Progesteron, aber auch voneinander unterscheiden. Je nach Abkömmling binden sie mehr oder weniger stark an Androgen-, Glukokortikoid-, Mineralokortikoid- und, seltener, an Estrogenrezeptoren. Dort können sie agonistisch oder antagonistisch wirken. Entsprechend ihrer chemischen Struktur und ihrer räumlichen Ähnlichkeit mit dem jeweiligen natürlichen Steroid (z.B. Estradiol, Testosteron, Kortisol, Aldosteron) können Gestagene also als schwache Androgene oder Antiandrogene, als Glukokortikoide oder als Antimineralokortikoide wirken. Dies erklärt ihr jeweils unterschiedliches Wirkspektrum (s. Tab. 1).1,2
Tab. 1: Hormonelle Aktivitäten von Gestagenen. Modifiziert nach Gobrecht-Keller 2021.2
Wie Progesteron verfügen alle synthetischen Gestagene über eine antiestrogene Wirkung. Nahezu alle 19-Nortestosteron-Derivate besitzen zusätzlich eine androgene Partialwirkung. Eine Ausnahme ist Dienogest, welches chemisch zwar ein 19-Nortestosteron-Derivat ist, sich jedoch wie ein Abkömmling des Progesterons oder des 17α-OH-Progesterons verhält. Dienogest wirkt nicht androgen, sondern antiandrogen. Wenige synthetische Gestagene besitzen auch eine estrogene Restwirkung (s. Tab. 1).1,2
Somit können durch die Anwendung synthetischer Gestagene Effekte erzielt werden, die denen des natürlichen Progesterons ähneln. Durch die Wahl eines bestimmten synthetischen Gestagens können Patientinnen zudem von zusätzlichen Partialwirkungen profitieren. So kann sich beispielsweise bei Frauen mit Androgenisierungserscheinungen (z.B. Akne, Alopezie, Hirsutismus, Seborrhö) die Einnahme eines antiandrogen wirkenden kombinierten oralen Kontrazeptivums (KOK) positiv auf Haut und Haare auswirken. Hier wären z.B. KOK mit Dienogest, Chlormadinonacetat oder Drospirenon geeignet (s. Tab. 1).1,2,3
Im Folgenden werden beispielhaft zwei synthetische Gestagene im Detail vorgestellt.
Levonorgestrel
Levonorgestrel (LNG) zählt zu den 19-Nortestosteron-Derivaten. LNG ist ein potentes Gestagen ohne glukokortikoide und ohne antimineralokortikoide Partialwirkung, es besitzt jedoch eine geringe androgene Aktivität.1,2
Als Bestandteil kombinierter oraler Kontrazeptiva (KOK) gilt Levonorgestrel als zu bevorzugende Gestagenkomponente, da in Studien ein vergleichsweise geringes Risiko für thromboembolische Ereignisse aufgezeigt wurde.7,8,9 Zudem stehen in Deutschland ein orales Präparat („Minipille“) und sowie intrauterine Gestagenmonopräparate (Hormonspiralen) mit LNG in unterschiedlichen Dosierungen zur Kontrazeption zur Verfügung.3
Auch zur Notfallkontrazeption können LNG-haltige Gestagenmonopräparate eingesetzt werden – häufig bekannt als „Pille danach“.3
LNG wird außerdem als Gestagenkomponente im Rahmen einer kombinierten menopausalen Hormonersatztherapie (HRT) zur Endometriumprotektion eingesetzt.2
Mehr erfahren
Dienogest
Dienogest ist ebenfalls ein 19-Nortestosteron-Derivat und hat eine starke gestagene Partialwirkung. Üblicherweise verfügen 19-Nortestosteron-Derivate zusätzlich über eine androgene Partialwirkung. Dienogest stellt jedoch aufgrund seiner chemischen Struktur eine Ausnahme dar und ist das einzige Nortestosteron-Derivat, das nicht nur keine androgene, sondern eine antiandrogene Partialwirkung aufweist.1,2,4,10
Zur hormonellen Kontrazeption stehen verschiedene KOK mit Dienogest zur Verfügung. Eines ist auch zur Therapie von mittelschwerer Akne zugelassen.4,10
Dienogest ist zudem in der Behandlung der Endometriose etabliert – es dient insbesondere der Linderung Endometriose-bedingter Unterbauchschmerzen.4,5,10
Auch in kombinierten oralen HRT-Präparaten findet sich Dienogest als Gestagenkomponente zum Endometriumschutz.1,2,10
Mehr erfahren
-
Birkhäuser M. Klinische Bedeutung von gestagenen Partialwirkungen. Gynäkologische Endokrinologie 2006; 4:52–64.
-
Gobrecht-Keller U. Gestagengabe in der Menopause: Was sind Unterschiede, Vorteile und Nachteile der einzelnen Präparate? Journal für Gynäkologische Endokrinologie/Schweiz 2006; 24(4):1-9.
-
Wiegratz I. Hormonale Kontrazeption – was, wann, für wen? Dtsch Arztebl Int 2011; 108(28-29):495-506.
-
Bartsch V. Gynäkologische Anwendungen von Dienogest alleine und in Kombination mit Östrogenen. J Med Drug Rev 2020; 10:1–35.
-
Schäfer S. Indikationen zur medikamentösen Therapie bei Endometriose. gynäkologie + geburtshilfe 2020; 25:20–23.
-
Fachinformation Visanne® 2 mg Tabletten, Stand: April 2020.
-
Vinogradova et al. Use of combined oral contraceptives and risk of venous thromboembolism: nested case-control studies using the QResearch and CPRD databases. BMJ 2015; 350:h2135.
-
Dragoman MV et al. A systematic review and meta-analysis of venous thrombosis risk among users of combined oral contraception. Int J Gynaecol Obstet. 2018; 141(3):287-294.
-
Rote-Hand-Brief zu kombinierten hormonalen Kontrazeptiva: Verordnung solcher mit dem niedrigsten Risiko für venöse Thromboembolien und Nutzung des behördlich beauflagten Schulungsmaterials, 30.09.2021. Online unter: www.bfarm.de/SharedDocs/Risikoinformationen/Pharmakovigilanz/DE/RHB/2021/rhb-khk.html. Letzter Zugriff: 15.05.2024.
-
Gelbe Liste; Dienogest. Online unter: www.gelbe-liste.de/wirkstoffe/dienogest_18867. Letzter Zugriff: 13.05.2024.