HRT und Osteoporose/Knochenmineralhaushalt
Eine Estrogensubstitutionstherapie kann den postmenopausalen Knochenmasseverlust aufhalten1,2,3,4. Dies wurde mit verschiedenen Präparaten sowie verschiedenen Dosierungen und Anwendungsarten nachgewiesen. Auch der Fraktur-verhütende Effekt ist durch große Kohorten-Studien wie die Million-Frauen-Studie5,6 und prospektive randomisierte Studien wie der WHI7,8,9 für multiple, klinisch relevante Lokalisationen gut belegt.
Fraktur- und Osteoporoseprävention durch Hormontherapie
In der Million-Frauen-Studie6 wurde eine signifikante Verminderung der Frakturhäufigkeit um 25 % auch bei transdermaler Estradiolanwendung festgestellt. In der WHI-Studie war mit der eingesetzten Estrogen-Gestagen-Kombination bei einer Therapiedauer von durchschnittlich 5,6 Jahren die Häufigkeit von Frakturen im Vergleich zu Placebo um 24 % gesenkt, bei Hüftfrakturen betrug die Reduktion 33 % (konkret 11 Fälle versus 16 Fälle pro 10.000 Frauen und Jahr) und bei Wirbelfrakturen 35 % (konkret 11 Fälle versus 17 Fälle pro 10.000 Frauen und Jahr)7. Die Daten der Nachbeobachtungsphase zeigten, dass innerhalb von 5 Jahren nach Therapieende die Frauen, die in der Behandlungsphase ausschließlich CEE (konjugierte Stutenestrogene) eingenommen hatten, eine geringere Gesamt-Frakturrate im Vergleich zu den Placebo-Anwenderinnen aufwiesen. Keine Verringerung der Gesamt-Frakturrate und der Anzahl von Hüftfrakturen fand sich allerdings in der Gruppe, die CEE und MPA (Medroxyprogesteronacetat) verwendet hatten10.
Dosierung und transdermale Anwendung
In mehreren Studien konnte gezeigt werden, dass auch die transdermale Anwendung von Estrogen den Knochenmasseverlust effizient verhindern kann11,12,13,14,15. In einer Metaanalyse, in der Daten aus neun Studien zusammengefasst wurden, ergab sich ein geschätzter signifikanter Anstieg der Knochendichte um 3,4 % (95%-KI 1,7–5,1) nach einem und um 3,7 % (95%-KI 1,7–5,7) nach 2-jähriger transdermaler Estradiol-Behandlung. Eingesetzt wurden sowohl Pflaster, Gel als auch subkutane Implantate.
Schon sehr geringe Mengen an Estrogen reichen aus, um einen positiven Effekt auf den Knochenhaushalt zu bewirken. Es scheint dabei keinen bestimmten Schwellenwert zu geben, bei dem Estrogen seine Wirkung entfaltet, sondern eher eine Dosis-lineare Wirkbeziehung zu bestehen16. Beispielsweise reduzieren Estrogene in einer Standarddosierung die Marker für den Knochenumsatz um ca. 40–50 %. Niedrig dosierte Estrogene17,18 oder transdermales Estradiol19,20 hingegen um 25–30 %, während ultra-niedrig dosierte Estrogene noch ca. 20 % Reduktion der Knochenumsatzmarker bewirken können12,17. In verschiedenen Studien konnte zudem ein Zuwachs der Knochenmineraldichte mit niedrig dosiertem21 und ultra-niedrig dosiertem Estrogen12 gezeigt werden.
In einer Studie von Johnson et al. (2005)22 wurden postmenopausale Frauen 2 Jahre mit ultra-niedrig dosiertem Estradiol (14 µg/Tag) transdermal behandelt. In dem Behandlungszeitraum zeigten die Estradiol- und die Placebogruppe ähnliche Raten für Endometriumhyperplasie, -proliferation und vaginale Blutungen. Trotz Empfehlung eines Gestagenzusatzes bei vorhandenem Uterus23 scheint demnach diese Therapie zu keiner oder nur einer geringen Endometriumstimulation zu führen. Gleichzeitig bietet sie eine Option, dem Knochenverlust durch Reduzierung des Knochenumsatzes vorzubeugen (s. oben)12.
Zulassungsstatus und Anwendungsempfehlungen
Die Indikationsstellung einer HRT zur Osteoporoseprävention ist in Europa sehr restriktiv. Eine Behandlung ist nur bei postmenopausalen Frauen mit hohem Frakturrisiko vorgesehen, die gleichzeitig eine Unverträglichkeit oder Kontraindikation gegenüber anderen zur Osteoporoseprävention zugelassenen Arzneimitteln aufweisen24. Die internationale Menopausegesellschaft schreibt hingegen in ihren Empfehlungen3: „Die Wahl einer medikamentösen Therapie sollte auf Basis einer Abwägung von Wirksamkeit, Risiken und Kosten erfolgen. Die HRT ist die geeignetste Therapie zur Frakturprävention in der frühen Menopause.“ Die Nordamerikanische Menopausegesellschaft sowie die deutschsprachigen Wissenschaftlichen Osteologischen Gesellschaften schlossen sich im Gegensatz dazu in ihren aktuellen Empfehlungen der Indikationsstellung der europäischen Arzneimittelagentur an4,25.
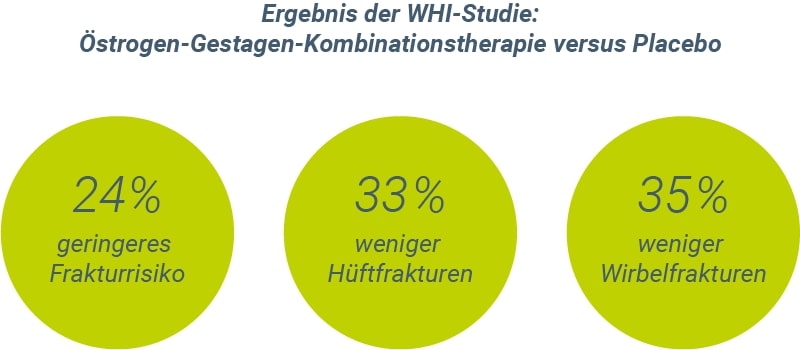
Abbildung 1: Vermindertes Frakturrisiko in der WHI-Studie bei Anwendung einer Kombinationstherapie mit konjugierten equinen Estrogenen und Medroxyprogesteronacetat über im Mittel 5,6 Jahre7.
-
Wells, G., et al. (2002, Aug). Meta-analyses of therapies for postmenopausal osteoporosis. V. Meta-analysis of the efficacy of hormone replacement therapy in treating and preventing osteoporosis in postmenopausal women. Endocr Rev, 23(4), pp. 529-39.
-
National Institute for Health and Care Excellence (NICE). (2015, Nov). NICE Guideline. Menopause: Diagnose and Management.
-
Baber, R., Panay, N., Fenton, A., & for the IMS Writing Group. (2016). IMS Recommendations on women's midlife health and menopause hormone therapy. Climacteric, 19(2), pp. 109-50.
-
NAMS (The North American Menopause Society). (2017, Jun). The 2017 hormone therapy position statement of The North American Menopause Society. Menopause: The Journal of The North American Menopause Society, 24(7), pp. 728-53.
-
Oursler, M., Landers, J., Riggs, B., & Spelsberg, T. (1993, Aug). Oestrogen effects on osteoblasts and osteoclasts. Ann Med, 25(4), pp. 361-71.
-
Banks, E., et al. (2004, May). Fracture incidence in relation to the pattern of use of hormone therapy in postmenopausal women. JAMA, 291(18), pp. 2212-20.
-
Cauley, J., et al. (2003, Oct). Effects of estrogen plus progestin on risk of fracture and bone mineral density: the Women's Health Initiative randomized trial. JAMA, 290(13), pp. 1729-38.
-
Jackson, R., et al. (2006, Jun). Effects of conjugated equine estrogen on risk of fractures and BMD in postmenopausal women with hysterectomy: results from the women's health initiative randomized trial. J Bone Miner Res, 21(6), pp. 817-28.
-
Manson, J., et al. (2013, Oct). Menopausal hormone therapy and health outcomes during the intervention and extended poststopping phases of the Women's Health Initiative randomized trials. JAMA, 310(13), pp. 1353-68.
-
Watts, N., et al. (2017, Jan). No Increase in Fractures After Stopping Hormone Therapy: Results From the Women's Health Initiative. J Clin Endocrinol Metab, 102(1), pp. 302-8.
-
Davas, et al., (2003). Effect of daily hormone therapy and alendronate use on bone mineral density in postmenopausal women. Fertil Steril. Vol. 80, 3, pp. 536-40.
-
Ettinger, et al., (2004). Effects of ultralow-dose transdermal estradiol on bone mineral density: a randomized clinical trial. Obstet Gynecol. Vol. 104, 3, pp. 443-51.
-
Yang, T., Chen, Y., Liang, W., Chang, C., Tai, L., Chang, S., & Ng, H. (2007, May). A clinical trial of 3 doses of transdermal 17beta-estradiol for preventing postmenopausal bone loss: a preliminary study. J Chin Med Assoc, 70(5), pp. 200-6.
-
Stanosz, S, et al., (2009). Influence of modified transdermal hormone replacement therapy on the concentrations of hormones, growth factors, and bone mineral density in women with osteopenia. Metabolism. Vol. 58, 1, pp. 1-7.
-
Kim, HJ, et al., (2014). Effect of transdermal estrogen therapy on bone mineral density in postmenopausal korean women. J Menopausal Med. Vol. 20, 3, pp. 111-7.
-
Ettinger, B. Rationale for use of lower estrogen doses for postmenopausal hormone therapy. Maturitas. May 2007, Vol. 57, 1, pp. 81-4. Gynäkologie, Menopause.
-
Prestwood, KM, et al., (2000) The effect of low dose micronized 17ss-estradiol on bone turnover, sex hormone levels, and side effects in older women: a randomized, double blind, placebo-controlled study. J Clin Endocrinol Metab. Vol. 85, 12, pp. 4462-9.
-
Lindsay, R, et al., (2002). Effect of lower doses of conjugated equine estrogens with and without medroxyprogesterone acetate on bone in early postmenopausal women. JAMA. Vol. 287, 20, pp. 2668-76.
-
Sharp, CA, et al., (1996). Effects of low- and conventional-dose transcutaneous HRT over 2 years on bone metabolism in younger and older postmenopausal women. Eur J Clin Invest. Vol. 26, 9, pp. 763-71.
-
Delmas, PD, et al., (2001). Three-year follow-up of the use of transdermal 17beta-estradiol matrix patches for the prevention of bone loss in early postmenopausal women. Am J Obstet Gynecol. Vol. 184, 2, pp. 32-40.
-
Peeyananjarassri, K and Baber, R. (2005). Effects of low-dose hormone therapy on menopausal symptoms, bone mineral density, endometrium, and the cardiovascular system: a review of randomized clinical trials. Climacteric. Vol. 8, 1, pp. 13-23.
-
Johnson, SR, et al., (2005) Uterine and vaginal effects of unopposed ultralow-dose transdermal estradiol. Obstet Gynecol. Vol. 105, 4, pp. 779-87.
-
3M Pharmaceuticals. Menostar®. Prescription Information. USA : s.n., 2006. Gynäkologie, Menopause.
-
Co-ordination Group for Mutual Recognition and Decentralised procedures - Human (CMDh). (2017, Feb). CORE SmPC for Hormone Replacement Therapy Products.
-
Dachverband der Deutschsprachigen Wissenschaftlichen Osteologischen Gesellschaften e.V. Prophylaxe, Diagnostik und Therapie der Osteoporose. DVO-Leitlinie Osteoporose 2014. 2014.