Verlauf der Wechseljahre
Mit Beginn der Wechseljahre steigt die Prävalenz für Osteoporose, Diabetes, kardiovaskuläre Erkrankungen und metabolisches Syndrom.
Welche Langzeitfolgen können im Verlauf der Wechseljahre auftreten?
Estrogene und Progesteron spielen nicht nur im Rahmen der Fortpflanzung eine wichtige Rolle sondern haben auch weitreichenden Einfluss auf Muskeln, Bindegewebe und Blutgefäße. Anders als die kurzfristigen Folgen des Hormonmangels in den Wechseljahren, wie Hitzewallungen, Schlafstörungen und depressive Verstimmungen, die sich sehr rasch bemerkbar machen, treten die Langzeitfolgen erst allmählich in Erscheinung.
Das Osteoporose-Risiko steigt in den Wechseljahren deutlich an
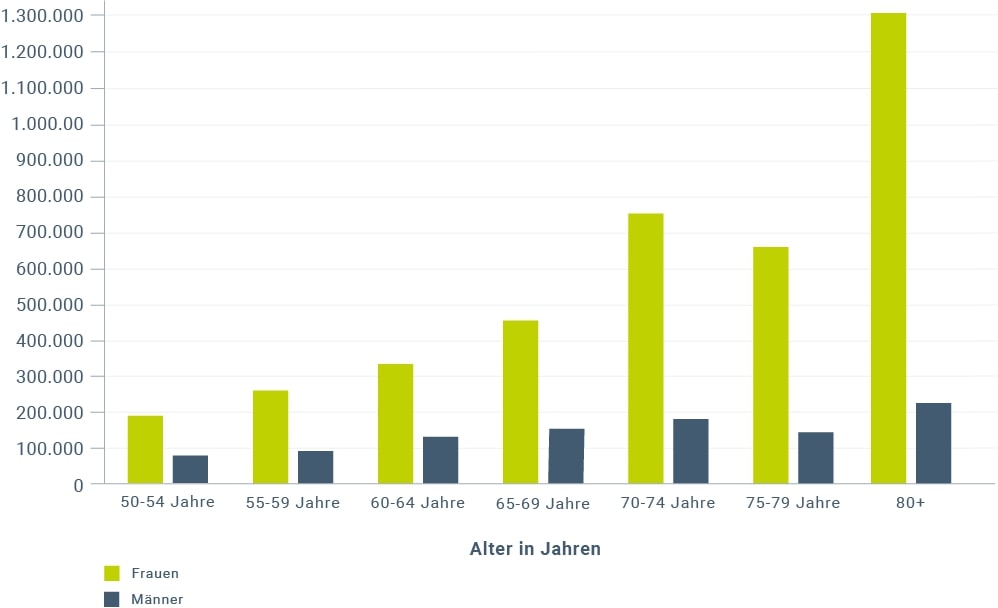
Bereits in der Perimenopause setzt ein beschleunigter Knochenmasseverlust ein1, der postmenopausal zu einer Osteoporose mit erhöhter Frakturanfälligkeit führen kann2,3. Die Häufigkeit von Frakturen der Extremitäten ist bei Frauen bis zum 54. Lebensjahr zwar jener bei Männern vergleichbar, um sich dann aber rasch dramatisch zu steigern und erst bei den über 80-Jährigen findet wieder eine Annäherung der Häufigkeiten zwischen den Geschlechtern statt4.
2010 litten in der Europäischen Union 22 Millionen Frauen und 5,5 Millionen Männer an Osteoporose5. Es wird erwartet, dass die jährliche Zahl an Knochenbrüchen von 3,5 Millionen im Jahr 2010 auf 4,5 Millionen in 2025 steigt, was einen Anstieg um 28 % bedeuten würde6. Für Deutschland wird geschätzt, dass fast ein Viertel der 50- bis 64-jährigen sowie mehr als die Hälfte der über 65-jährigen Frauen eine Osteoporose aufweist7.
Abbildung 1: Geschätzte Anzahl Frauen und Männer mit Osteoporose in Deutschland 2010 (T-Score ≤ -2,5 SD des Femurhalses) (modifiziert nach Svedbom et al. 20135).
Urogenitale Atrophie in den Wechseljahren
Informationen zur urogenitalen Atrophie in den Wechseljahren (urogenitales Menopausensyndrom) inklusive Symptome, Diagnose und Therapie finden Sie > hier.
Verschiedene Risikofaktoren erhöhen das Auftreten von kardiovaskulären Erkrankungen in den Wechseljahren
Wenngleich Frauen im Vergleich zu Männern später betroffen sind8,9,10, entwickeln sich in den postmenopausalen Jahren verstärkt kardiovaskuläre Erkrankungen wie Herzinfarkt und Schlaganfall, wobei erhöhter Blutdruck, abnorme Blutlipidwerte, Tabakgenuss, zu wenig körperliche Betätigung, Diabetes mellitus, die Ernährungsweise und Adipositas zu den wichtigsten modifizierbaren Risikofaktoren zählen11.
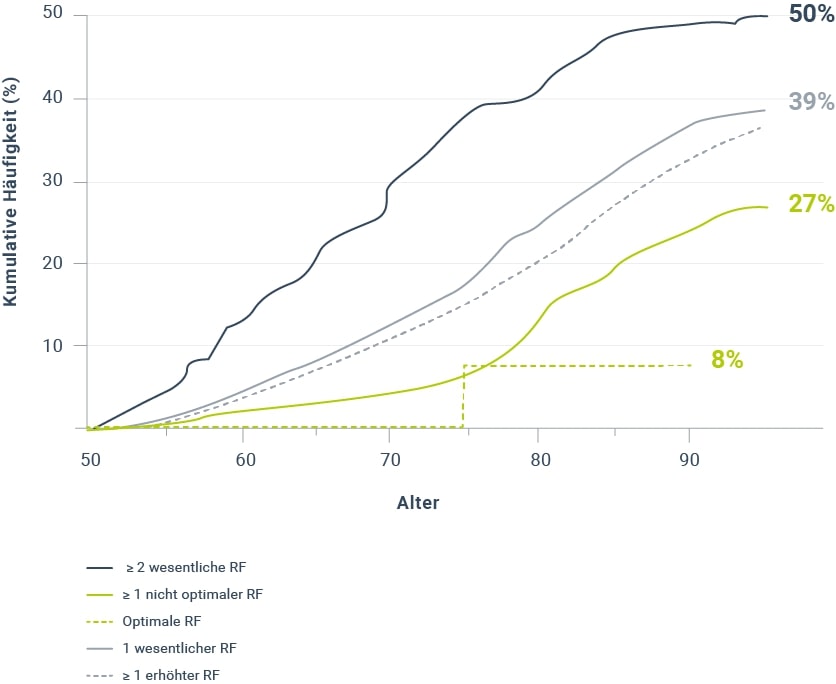
Jüngere12 sowie peri- und früh postmenopausale9,13 Frauen ohne relevante kardiovaskuläre Risikofaktoren haben ein sehr geringes Risiko für Herz-Kreislauf-Krankheiten (Abb. 2) und eine sehr hohe Lebenserwartung, allerdings bilden sie eine Minderheit. Bei Frauen mit prämaturer Menopause hingegen ist das Risiko für Herz-Kreislauf-Erkrankungen deutlich erhöht14. Diabetes Typ II15,16 sowie ein metabolisches Syndrom17,18 sind ebenfalls mit einem erheblich erhöhten kardiovaskulären Risiko assoziiert. Estrogene scheinen hingegen protektiv gegen Arteriosklerose zu wirken19,20,21.
Abbildung 2: Kumulative Häufigkeit kardiovaskulärer Erkrankungen von Frauen nach der Menopause in Abhängigkeit vom Profil kardiovaskulärer Risikofaktoren (RF) im Alter von 50 Jahren (modifiziert nach Lloyd-Jones et al. 200613).
Während im Alter bis 45 Jahre die Prävalenz einer Hypertonie bei Frauen niedriger ist als bei Männern, ist sie ab einem Alter von 55 Jahren bei Frauen höher im Vergleich zu Männern22. In der globalen Fall-Kontroll-Studie INTERHEART23 zum erstmaligen Auftreten eines Herzinfarktes wurde der Vorteil von Frauen im Vergleich zu Männern verdeutlicht: Während Männer weltweit im Median von 56 Jahren bzw. in Westeuropa im Median von 61 Jahren einen Erstinfarkt erleiden, betrifft dies Frauen weltweit erst im Alter von 65 Jahren, ein Vorteil von im Mittel 9 Jahren, bzw. in Westeuropa erst im Alter von 68 Jahren, ein Vorteil von im Mittel 7 Jahren.
Die Prävalenz für das metabolische Syndrom steigt in den Wechseljahren
Metabolisches Syndrom bezeichnet eine Cluster-Bildung spezifischer kardiovaskulärer Risikofaktoren, die Hauptdimensionen sind Übergewicht (insbesondere viszerale Adipositas, gekennzeichnet durch vermehrten Bauchumfang), Insulinresistenz, Dyslipidämie sowie arterielle Hypertonie24. Bei der Diagnose eines Risikofaktors sollte gezielt auch das Vorliegen weiterer Faktoren abgeklärt werden. Dabei sind zusätzlich insbesondere LDL-Cholesterin, Rauchen und Familienanamnese, aber auch erhöhte Thromboseneigung und eventuell erhöhte Entzündungsparameter zu beachten25. Wie generell in der kardiovaskulären Prävention bilden Änderungen des Lebensstils die Basis aller Interventionen25,26.
Wenngleich in geringerem Umfang als Alter und Übergewicht, so war bei Frauen auch ein postmenopausaler (im Vergleich zum prämenopausalen) Status mit einem um 60 % signifikant erhöhten Risiko für ein metabolisches Risiko assoziiert27. Eine Auswertung der SWAN(Study of Women’s Health Across the Nation)-Studie, der größten Kohortenstudie mit Frauen mittleren Alters, kam zu dem Ergebnis, dass die Prävalenz des metabolischen Syndroms während der Peri- und Postmenopause signifikant ansteigt, unabhängig vom Alter und anderen kardiovaskulären Risikofaktoren wie Gewichtszunahme und Rauchen28.
Die Häufigkeit des Typ-II-Diabetes nimmt in den Wechseljahren stark zu
Der Diabetes mellitus umfasst eine Gruppe von Krankheiten, deren gemeinsames Charakteristikum der chronisch erhöhte Blutzucker im Nüchternzustand oder nach Einnahme von Mahlzeiten (Hyperglykämie) ist29. Die Blutzuckererhöhung lässt sich durch Bestimmung der Blutzuckerkonzentration (nüchtern oder nach Glukosebelastung) nachweisen. Etwa 80–90 % aller Diabetes-Fälle gehören zum Typ II, der durch eine Insulinresistenz und/oder einen Insulinsekretionsdefekt gekennzeichnet ist. Die Häufigkeit des Typ-II-Diabetes nimmt mit dem Alter, ab etwa dem 40. Lebensjahr, stark zu, wobei sich die Mehrheit der betroffenen Frauen in der Postmenopause befindet. In Deutschland ist die Anzahl Erwachsener mit Diabetes von 3,4 Millionen Erkrankter in 1980 auf 5,1 Millionen in 2014 gestiegen30. Bereits 2004 wurde durch Daten aus einer hessischen Stichprobe31 in Deutschland (wie bereits in früheren Jahren in den USA32) von einer hohen Prävalenz des Typ-II-Diabetes ausgegangen. Bereits ab einem Alter von 50 Jahren sind ca. 10 % und mehr der Frauen betroffen.
Bedrohlich ist der Typ-II-Diabetes vor allem aufgrund seiner Folgeschäden, wobei Makro- (Herzinfarkt, Schlaganfall) und Mikroangiopathien (Nephropathie, Retinopathie) an erster Stelle stehen29.
Welchen Einfluss die Menopause unabhängig vom Alter auf die Glukosehomöostase hat, wird derzeit noch diskutiert33. Die Mehrzahl an Studien spricht allerdings für einen Einfluss der menopausalen Estrogendefizienz auf das erhöhte Typ-II-Diabetes-Risiko bei postmenopausalen Frauen34. Obgleich z. B. frühere Auswertungen der SWAN-Studie Änderungen in der Glukosehomöostase lediglich mit dem chronologischen Alter und nicht mit der Menopause per se assoziierten35,36, ließen spätere Auswertungen des Follow-ups andere Schlüsse zu37. Für einen Einfluss des ovariellen Alterns sprach bei Frauen mit niedrigeren Estrogenwerten während der frühen menopausalen Transition ein 47 % höheres Risiko an Typ-II-Diabetes zu erkranken. Auch wurde eine natürliche oder chirurgisch-induzierte prämature Menopause mit einem erhöhten Risiko für Typ-II-Diabetes assoziiert38,39.
Eine aktuelle Kohortenstudie mit 124.379 postmenopausalen Frauen der WHI-Studie zeigte, dass die kumulative Estrogenexposition (Differenz zwischen Alter bei Menarche und Menopause)40 das Risiko für die Erkrankung an Typ-II-Diabetes beeinflusst. Danach haben Frauen sowohl mit einer sehr kurzen (reproduktive Phase < 30 Jahre) als auch mit einer sehr langen Estrogenexposition (≥ 45 Jahre) ein erhöhtes Risiko, Typ-II-Diabetes zu entwickeln (37 bzw. 23 % höheres Risiko) als Frauen mit einer mittel langen reproduktiven Phase von 36–40 Jahren.
-
Finkelstein, J., et al. (2008, Mar). Bone mineral density changes during the menopause transition in a multiethnic cohort of women. J Clin Endocrinol Metab, 93(3), pp. 861-8.
-
Kanis, J., et al. (2013, Jan). European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos Int, 24(1), pp. 23-57.
-
NAMS (The North American Menopause Society). (2017, Jun). The 2017 hormone therapy position statement of The North American Menopause Society. Menopause: The Journal of The North American Menopause Society, 24(7), pp. 728-53.
-
Melton, L. (1988). Epidemiology of fractures. In B. Riggs, & L. (. Melton, Osteoporosis: etiology,diagnosis and management (pp. 225-247). New York: Raven Press.
-
Svedbom, A., et al. (2013). Osteoporosis in the European Union: a compendium of country-specific reports. Arch Osteoporos, 8, p. 137.
-
Hernlund, E., et al. (2013). Osteoporosis in the European Union: medical management, epidemiology and economic burden. A report prepared in collaboration with the International Osteoporosis Foundation (IOF) and the European Federation of Pharmaceutical Industry Associations (EFPIA). Arch Osteoporos, 8, p. 136.
-
Ziller, V., & Hadji, P. (2008). Leitliniengerechte Diagnostik und Therapie der postmenopausalen Osteoporose. Frauenarzt, 49, S. 424-36.
-
Kannel, W., & Wilson, P. (1995, Jan). Risk factors that attenuate the female coronary disease advantage. Arch Intern Med, 155(1), 57-61.
-
Stamler, J., et al. (1999). Low risk-factor profile and long-term cardiovascular and noncardiovascular mortality and life expectancy: findings for 5 large cohorts of young adult and middle-aged men and women. JAMA, 282(21), 2012-8.
-
ESHRE Capri Workshop Group. (2006, Sep-Oct). Hormones and cardiovascular health in women. Hum Reprod Update, 12(5), 483-97.
-
Vilahur, G., Badimon, J., Bugiardini, R., & Badimon, L. (2014). The burden of cardiovascular risk factors and coronary heart disease in Europe and worldwide. Eur Heart J, 16(Suppl A), pp. A7-A11.
-
Daviglus, M., et al., (2004, Oct). Favorable cardiovascular risk profile in young women and long-term risk of cardiovascular and all-cause mortality. JAMA, 292(13), pp. 1588-92.
-
Lloyd-Jones, D., et al., (2006, Feb). Prediction of lifetime risk for cardiovascular disease by risk factor burden at 50 years of age. Circulation, 113(6), pp. 791-8.
-
Faubion, S., Kuhle, C., Shuster, L., & Rocca, W. (2015). Long-term health consequences of premature or early menopause and considerations for management. Climacteric, 18(4), pp. 483-91.
-
NAMS (The North American Menopause Society). (2000, Mar-Apr). Effects of menopause and estrogen replacement therapy or hormone replacement therapy in women with diabetes mellitus: consensus opinion of The North American Menopause Society. Menopause, 7(2), pp. 87-95.
-
Wedisinghe, L., & Perera, M. (2009, Jul). Diabetes and the menopause. Maturitas, 63(3), pp. 200-3.
-
Eckel, R., Grundy, S., & Zimmet, P. (2005, Apr). The metabolic syndrome. Lancet, 365, pp. 1415-28.
-
Lobo, R. (2008, May). Metabolic syndrome after menopause and the role of hormones. Maturitas, 60(1), pp. 10-8.
-
Mendelsohn, M., & Karas, R. (2005, Jun). Molecular and cellular basis of cardiovascular gender differences. Science, 308(5728), pp. 1583-7.
-
Manson, J., et al. (2007). Estrogen therapy and coronary-artery calcification. N Engl J Med, 356(25), pp. 2591-602.
-
Mikkola, T., Savolainen-Peltonen, H., Venetkoski, M., & Ylikorkala, O. (2017, Feb). New evidence for cardiac benefit of postmenopausal hormone therapy. Climacteric, 20(1), pp. 5-10.
-
Oparil, S., et al. (1997). Sexually dimorphic response of the balloon-injured rat carotid artery to hormone treatment. Circulation, 95(5), pp. 1301-7.
-
Yusuf, S., et al., (2004, Sep). Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART study): case-control study. Lancet, 364(9438), pp. 937-52.
-
Alberti, K., et al., (2009, Oct). Harmonizing the metabolic syndrome: a joint interim statement of the International Diabetes Federation Task Force on Epidemiology and Prevention; NHLBI; AHA; WHF; IAS; IASO. Circulation, 120(16), pp. 1640-5.
-
Grundy, S., et al., (2005, Oct). Diagnosis and management of the metabolic syndrome: an American Heart Association/National Heart, Lung, and Blood Institute Scientific Statement. Circulation, 112(17), pp. 2735-52.
-
Park, Y., et al., (2003, Feb). The metabolic syndrome: prevalence and associated risk factor findings in the US population from the Third National Health and Nutrition Examination Survey, 1988-1994. Arch Intern Med, 163(4), pp. 427-36.
-
Janssen, I., et al. (2008, Jul). Menopause and the metabolic syndrome: the Study of Women's Health Across the Nation. Arch Intern Med, 168(14), pp. 1568-75.
-
Icks, A., et al., (2005). Diabetes mellitus. Gesundheitsberichterstattung des Bundes(24). Robert-Koch-Institut.
-
NCD Risk Factor Collaboration (NCD-RisC). (2016, Apr). Worldwide trends in diabetes since 1980: a pooled analysis of 751 population-based studies with 4.4 million participants. Lancet, 387(10027), pp. 1513-30.
-
Hauner, H., Köster, I., & Schubert, I. (2007). Trends in der Prävalenz und ambulanten Versorgung von Menschen mit Diabetes mellitus. Dtsch Arztebl(104), S. A2799-805.
-
Harris, M., et al., (1998, Apr). Prevalence of diabetes, impaired fasting glucose, and impaired glucose tolerance in U.S. adults. The Third National Health and Nutrition Examination Survey, 1988-1994. Diabetes Care, 21(4), pp. 518-24.
-
Karvonen-Gutierrez, C., Park, S., & Kim, C. (2016, Apr). Diabetes and Menopause. Curr Diab Rep, 16(4), p. 20.
-
Mauvais-Jarvis, F., Manson, J., Stevenson, J., & Fonseca, V. (2017, Jun). Menopausal Hormone Therapy and Type 2 Diabetes Prevention: Evidence, Mechanisms, and Clinical Implications. Endocr Rev, 38(3), pp. 173-88.
-
Matthews, K., et al. (2009, Dec). Are changes in cardiovascular disease risk factors in midlife women due to chronological aging or to the menopausal transition? J Am Coll Cardiol, 54(25), pp. 2366-73.
-
Matthews, K., Gibson, C., El Khoudary, S., & Thurston, R. (2013, Jul). Changes in cardiovascular risk factors by hysterectomy status with and without oophorectomy: Study of Women's Health Across the Nation. J Am Coll Cardiol, 62(3), pp. 191-200.
-
Park, S., et al. (2017, Apr). Association between changes in oestradiol and follicle-stimulating hormone levels during the menopausal transition and risk of diabetes. Diabet Med, 34(4), pp. 531-8.
-
Brand, J., et al. (2013, Apr). Age at menopause, reproductive life span, and type 2 diabetes risk: results from the EPIC-InterAct study. Diabetes Care, 36(4), pp. 1012-9.
-
Appiah, D., Winters, S., & Hornung, C. (2014). Bilateral oophorectomy and the risk of incident diabetes in postmenopausal women. Diabetes Care, 37(3), pp. 725-33.
-
LeBlanc, E., et al. (2017, Jan). Reproductive history and risk of type 2 diabetes mellitus in postmenopausal women: findings from the Women's Health Initiative. Menopause, 24(1), pp. 64-72.